
DOI: 10.1016/j.xplc.2026.101736
2026年1月21日,果蔬园艺作物种质创新与利用国家重点实验室曾云流团队在Plant Communications发表了题为“A cool temperature-induced ubiquitination-controlled transcription factor promotes starch degradation and ripening in kiwifruit”的研究论文。该研究阐明了猕猴桃在低温(5-10 ℃)条件下,不依赖于乙烯信号通路即可启动淀粉降解和果实成熟的分子机制,为果实成熟过程中温度控制下的淀粉降解提供了理论基础。
研究背景
淀粉作为果实中重要的储能物质,其降解转化为糖分直接影响果实风味与食用品质。淀粉代谢主要受乙烯调控,同时还受温度、光照和营养等环境因素的影响。猕猴桃等呼吸跃变型果实的成熟高度依赖乙烯信号。然而,生产中依赖外源乙烯催熟易导致果实过度软化、货架期缩短。近年研究发现,特定低温条件可绕过乙烯通路促进果实成熟,但其分子机制一直未被揭示。
研究内容
研究团队首先通过生理测定发现,在利用1-甲基环丙烯(1-MCP)阻断乙烯感知的前提下,与室温(20 ℃)或冷藏(1 ℃)相比,5-10 ℃的低温(CT)处理能显著促进三个不同果肉颜色猕猴桃品种(“金塘三号”、“红阳”和“翠香”)的软化、淀粉降解及可溶性固形物含量上升(图1)。代谢组学分析进一步证实,低温诱导的成熟具有独特的代谢谱,与乙烯处理既存在部分重叠(如淀粉降解产物),也存在显著差异(图1C),证明了存在一条独立于乙烯的低温诱导成熟通路。

图1 经1-MCP处理的猕猴桃在不同温度贮藏期间的生理与代谢物变化
为揭示低温诱导的猕猴桃成熟过程中淀粉降解的分子机制,研究团队进行了转录组学分析,并鉴定到一个在低温下特异性上调表达的β-淀粉酶基因AcBAM3.3(图2A-D)。功能验证表明,AcBAM3.3及其同源基因AcBAM3.5具有降解淀粉的活性,在猕猴桃愈伤组织和番茄果实中过表达这些基因能显著降低淀粉含量(图2F)。这说明AcBAM3s是低温诱导淀粉降解的关键酶。

图2 猕猴桃在低温与乙烯处理下成熟过程中的转录组数据及淀粉代谢相关基因表达
通过转录因子筛选,研究团队鉴定到一个低温特异性高表达的ERF家族转录因子AcCTS1(Cool Temperature Specific 1)。双荧光素酶报告基因(LUC)、酵母单杂交(Y1H)、电泳迁移率变动分析(EMSA)试验证实,AcCTS1能够直接结合到AcBAM3.3和AcBAM3.5的启动子特定区域(DRE元件),并激活它们的转录(图3A-F)。在猕猴桃愈伤组织和果实中,过表达AcCTS1促进淀粉降解,而利用CRISPR-Cas9技术敲除AcCTS1则显著抑制了低温诱导的淀粉降解(图4),证实了AcCTS1是该通路的核心正调控因子。

图3 AcCTS1激活AcBAM3.3和AcBAM3.5的表达

图4 AcCTS1调控猕猴桃低温诱导的淀粉降解
那么,AcCTS1的活性如何在常温下被抑制,又在低温下被激活?通过酵母双杂交(Y2H)筛选,研究团队找到了一个E3泛素连接酶AcPUB11。一系列体内外实验(酵母双杂、荧光互补、Co-IP等)证实了两者的直接互作(图5A-E)。在室温下,AcPUB11丰度较高,它能够与AcCTS1结合,介导其泛素化修饰,进而通过26S蛋白酶体途径降解AcCTS1,从而抑制下游AcBAM3基因的表达和淀粉降解,维持淀粉稳定(图5)。然而,在低温条件下,AcPUB11的蛋白丰度显著下降(尽管其转录水平上升),这导致AcCTS1得以积累和稳定存在。积累的AcCTS1进而激活AcBAM3.3/3.5,驱动淀粉转化为糖,诱导果实成熟(图6)。

图5 AcPUB11与AcCTS1互作并泛素化修饰AcCTS1,促使其通过蛋白酶体降解

图6 AcPUB11削弱AcCTS1介导的淀粉降解
研究结论
综上所述,该研究揭示了低温(5-10 ℃)通过AcPUB11-AcCTS1-AcBAM3s模块调控猕猴桃中与乙烯无关的淀粉降解和成熟过程。在室温条件下,AcPUB11会促使AcCTS1通过蛋白酶体途径被降解;然而,在低温条件下,AcPUB11的含量会减少,从而使AcCTS1能够激活AcBAM3.3/3.5并启动淀粉水解和成熟过程(图7)。这项研究为温度介导的采后品质调控提供了分子框架。
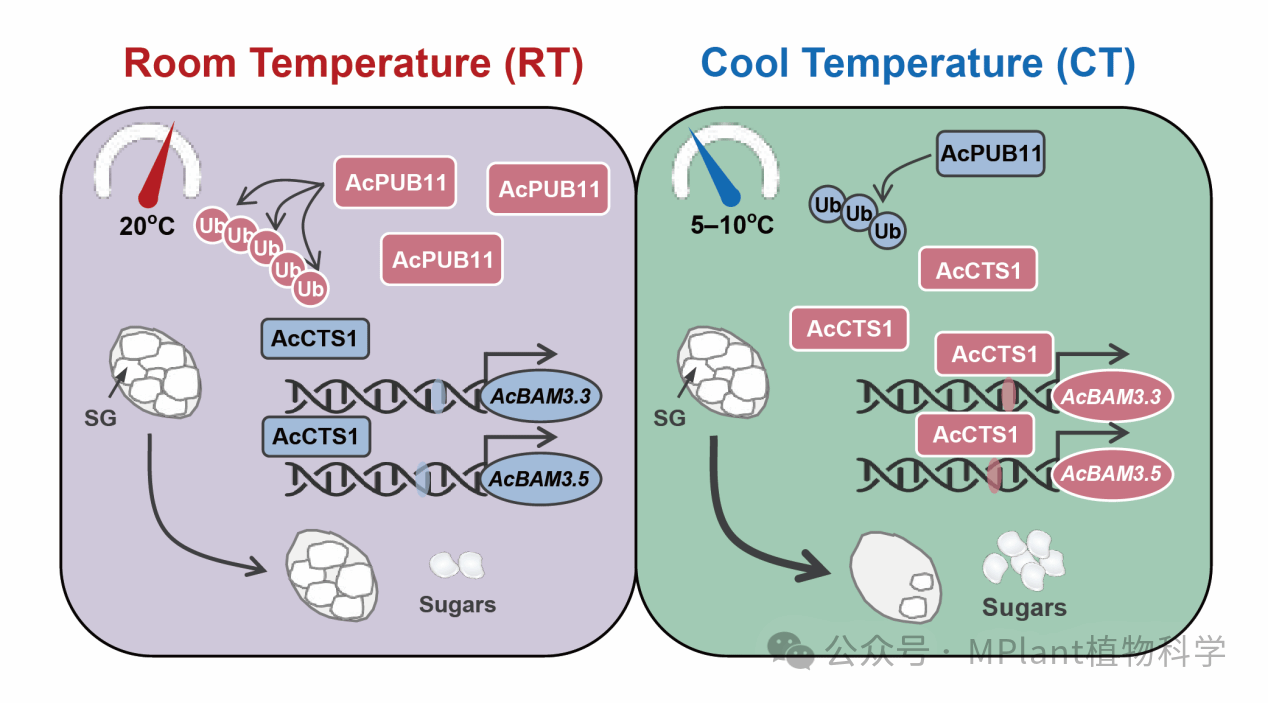
图7 猕猴桃在乙烯抑制条件下低温诱导淀粉降解的调控网络模型
本文转自公众号MPlant植物科学(Plant Com | 华中农业大学曾云流团队揭示猕猴桃在低温下诱导成熟的分子机制)

